Governo de SP define data para início de vacinação, mas deixa interrogações no ar

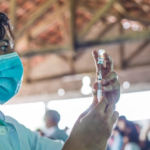
Doria com um frasco da CoronaVac, em outubro, no Senado (Foto: Governo de São Paulo via FotosPúblicas)
O governador João Doria anunciou em entrevista coletiva no começo da tarde desta segunda-feira, 7 de dezembro, no Palácio dos Bandeirantes, que a vacinação contra a covid-19 começará no estado de São Paulo em 25 de janeiro, independentemente da decisão do governo federal quanto à data de início da campanha nacional. Até o momento, o Ministério da Saúde vem dizendo que começará a vacinação em todo o país em março de 2021.
A notícia dada no Morumbi seria, de fato, excelente se não estivesse assentada em terreno acidentado, ainda permeado por dúvidas e interrogações sobre o produto que será usado, a CoronaVac, vacina desenvolvida pela empresa chinesa Sinovac em parceria, no Brasil, com o Instituto Butantan.
A primeira dúvida/interrogação diz respeito a quando teremos, enfim, os resultados da fase 3 dos testes clínicos. E a segunda refere-se ao tempo que a Agência Nacional de Vigilância Sanitária (Anvisa), gastará, uma vez de posse dos resultados finais, para dar seu aval quanto à qualidade, do produto principalmente em termos de segurança e eficácia, equivalente a uma autorização para que se comece efetivamente a vacinação.
“Tomara que tenhamos a vacinação como anunciada. Temos o plano, a agenda, mas ainda não a vacina”, pondera Jorge Kalil, professor titular de Imunologia Clínica da Faculdade de Medicina da Universidade de São Paulo (FM-USP) e diretor do Laboratório de Imunologia do Incor, em entrevista ao Ciência na rua. Por ter a vacina ele quer dizer exatamente ela ter sido bem avaliada pela Anvisa, depois de divulgados seus resultados de eficácia e toxicidade, entre outros parâmetros.
Expectativas positivas
Em principio, há uma expectativa de que ainda nesta semana ou começo da outra o governo paulista tenha um retorno quanto à eficácia da CoronaVac por parte do comitê independente que a define (DSMC, sigla de Data and Safety Monitoring Committee), com base nos números obtidos na fase 3 dos testes clínicos. E isso porque, já na semana passada, o governo anunciara que tinha enviado os dados para o comitê e acreditava numa resposta até 15 de dezembro – tinha então atingido o número mínimo de infectados para cálculo da eficácia, dentro dos 13.500 voluntários de seu estudo. Se realmente for assim, a Anvisa terá pouco mais de um mês para sua avaliação, o que parece suficiente no regime de urgência que, ainda nesta segunda-feira, o diretor do Instituto Butantan, Dimas Covas, reafirmou que solicitará à agência.
Protocolos de testes de produtos farmacêuticos como vacinas têm, às vezes, 10 mil ou 15 mil páginas para serem examinadas. Mas há que se considerar, no caso da CoronaVac, que ela tem por base uma rota tecnológica largamente conhecida, baseada no uso do vírus atenuado, em que o próprio Butantan tem vasta experiência. Isso deve ser um complicador a menos na avaliação da Anvisa, ainda que, na prática, talvez resulte em menor eficácia da Coronavac do que os festejados 95% obtidos pelos produtos da Pfizer e da Moderna, baseados em tecnologia de RNA mensageiro. Há, em especial, uma grande expectativa quanto à eficácia do produto Sinovac-Butantan em relação aos maiores de 60 anos, uma vez que já se falou bastante de sua segurança.
Como há em torno da questão da vacinação no Brasil pesadas disputas políticas, incluindo uma aberta queda de braço entre o presidente da república e o governador de São Paulo, os prazos também respondem a imprevisíveis jogos de pressão nesse campo, mesmo que se esteja pondo em risco, com isso, a vida de milhares de brasileiros.
Admitido que tudo caminhe civilizadamente, a vacinação atingirá de 25 de janeiro a 22 de março o total de 9 milhões de pessoas dos grupos mais vulneráveis no estado de São Paulo (ver tabela abaixo), em 645 municípios. Além disso, serão oferecidas doses para a vacinação de 4 milhões de profissionais de saúde em outros estados. A logística da vacinação vai mobilizar 10 mil locais, agregando-se às 4.700 Unidades Básicas de Saúde, farmácias, quartéis, escolas, terminais de ônibus e o sistema de drive thru. O plano prevê o trabalho de 54 mil profissionais de saúde, 25 postos de distribuição e 5.200 câmaras de refrigeração, além de 30 caminhões climatizados, ao custo de R$ 100 milhões.