Herton Escobar, Jornal da USP
Reportagem acompanhou um dia de trabalho no laboratório de alta segurança da Plataforma Científica Pasteur-USP

Duas luvas de borracha em cada mão (a primeira delas selada ao punho com fita adesiva), máscara bem colada ao rosto, óculos, touca para os cabelos, três camadas de proteção nos pés e um macacão impermeável de corpo inteiro, com o capuz fechado até o queixo. Esse tem sido o uniforme básico de trabalho para um grupo de jovens pesquisadores na Plataforma Científica Pasteur-USP (PCPU), desde que a pandemia do novo coronavírus chegou ao Brasil.
Inaugurada em julho de 2019, no Centro de Inovação e Pesquisa da USP (Inova USP), a plataforma foi planejada para atuar justamente como uma “célula de intervenção rápida” contra vírus, bactérias e outros agentes infecciosos emergentes que representem uma ameaça à saúde pública. A primeira emergência não demorou a aparecer. Os equipamentos necessários para ocupar os 17 laboratórios da plataforma chegaram no início deste ano e terminaram de ser instalados no dia 13 de março, literalmente às vésperas da eclosão da epidemia do SARS-CoV-2 na cidade de São Paulo.
“Tivemos que reagir rapidamente e botar a plataforma para funcionar”, diz a biomédica Paola Minoprio, coordenadora da PCPU e diretora de pesquisa no Departamento de Saúde Global do Instituto Pasteur, em Paris. Todos os projetos de pesquisa originalmente previstos para ocupar a plataforma foram temporariamente suspensos, para centrar esforços no combate ao coronavírus. “Colocamos todos os nossos projetos de lado e falamos: Como é que a gente pode contribuir agora, com o que a gente tem na mão?”
Desde então, a plataforma integra uma grande rede de laboratórios da USP, cuja infraestrutura e expertise foram mobilizadas em caráter emergencial para dar suporte ao poder público na realização de exames moleculares do novo coronavírus — a Rede USP para o Diagnóstico da Covid-19 (RUDIC), com cinco núcleos de testagem espalhados pela capital e interior do Estado. “A prioridade agora é salvar vidas”, resume Paola.
No caso da PCPU, a incumbência é testar pacientes internados e profissionais de saúde do Hospital Universitário (HU) e do Hospital das Clínicas da Faculdade de Medicina da USP, que estão na linha de frente do atendimento à população.
As amostras chegam todo dia de manhã, por volta das 9h: três pedacinhos de algodão, mergulhados numa solução salina, dentro de um tubo plástico, envolto por um saco plástico, e transportado dentro de uma caixa térmica com gelo seco.
Os pedacinhos de algodão são as pontas dos cotonetes (ou swabs) que os médicos utilizam para coletar amostras de muco do interior das narinas e da garganta dos pacientes. E a solução salina (soro fisiológico) é o que os cientistas vão usar para detectar a presença do vírus nas amostras, se ele estiver lá.
Os primeiros exames foram feitos no dia 20 de março, com dois pacientes do HU: uma senhora de 92 anos e um senhor, de 63 — ambos negativos para o vírus. Na sequência, dia 23, mais sete pacientes, com quatro positivos. Até agora no total, cerca de 70 pessoas testadas.

Laboratório NB3, onde são processadas as amostras para diagnóstico molecular — Foto: Reprodução
Biossegurança
Os tubos com as amostras só são abertos dentro de um laboratório especial, categoria NB3 (Nível de Biossegurança 3, numa escala que vai de 1 a 4), respeitando uma série de regras rígidas de proteção física e operacional. É um ambiente completamente isolado do meio externo, projetado para impedir o escape de qualquer coisa que esteja sendo estudada dentro dele, por mais microscópica que seja. Nada entra nem sai de lá sem passar por um processo de descontaminação.
Os equipamentos de proteção individual (EPIs) que os pesquisadores vestem para trabalhar são todos descartáveis, com exceção dos óculos. O que não significa que sejam baratos; o kit individual completo custa cerca de R$ 120 — ou seja, um gasto semanal de, no mínimo, R$ 600 por pessoa, só para entrar no laboratório. A roupa é quente, desconfortável, e o trabalho exige um nível de concentração elevado (sem falar que não dá para ir ao banheiro, nem comer nem beber nada lá dentro, porque a máscara não pode ser removida em nenhum momento). Por isso, os turnos são limitados a quatro horas, e só é permitido trabalhar em duplas, para evitar que o cansaço gere desatenção e aumente o risco de acidentes.
“Trabalhamos com as mais rígidas regras de biossegurança”, garante Pedro Teixeira, gestor de biossegurança da PCPU e pesquisador da Fundação Oswaldo Cruz (Fiocruz), que também é parceira da plataforma.
A PCPU tem quatro laboratórios desse tipo — “os melhores da América Latina”, segundo Paola. Os encarregados de processar as amostras e fazer os testes são três jovens virologistas, pós-doutorandos da plataforma: Ana Paula Vilela, Angélica Campos e Marielton Cunha. “Se a gente não limitasse o tempo deles dentro do NB3, eles ficariam o dia inteiro lá”, elogia Teixeira. “Tá todo mundo querendo trabalhar.”
“De um dia para outro botamos isso aqui para funcionar, e agora estamos fazendo diagnóstico com qualidade e gerando pesquisas”, diz Angélica, que estuda vírus respiratórios (de seres humanos e morcegos) e se apresentou como voluntária para ajudar no trabalho. Os resultados dos exames saem em menos de 24 horas, com índice de acerto próximo de 100%.

Hall de acesso aos laboratórios NB3 da plataforma. Câmeras mostram o que acontece lá dentro — Foto: Herton Escobar/USP Imagens
Necessidade
A velocidade e a confiabilidade dos testes moleculares são essenciais para orientar a conduta dos médicos nos hospitais em meio à pandemia. Os sintomas da covid-19 são muito semelhantes aos de uma gripe (do vírus influenza) e outras infecções respiratórias, que são tratadas de forma diferente e não exigem que o paciente seja mantido em isolamento. Como o número de leitos é limitado, é fundamental saber o que o paciente realmente tem, o mais rápido possível, para não ocupar uma vaga de UTI sem necessidade, nem excluir alguém que realmente precise dela.
“Esses dias uma médica do HU me ligou às oito da noite para perguntar se a gente já tinha o resultado do exame, porque ela precisava liberar o leito com urgência”, relata Ana Paula, uma das responsáveis pelo trabalho na PCPU. Apesar da semelhança com outras infecções mais corriqueiras, a covid-19 pode evoluir rapidamente para quadros graves de pneumonia, em que o acesso a um ventilador mecânico pode fazer a diferença entre a vida e a morte para o paciente.
“Essa colaboração está sendo muito importante para nós”, diz a médica infectologista Valéria Cassettari, coordenadora do Controle de Infecção Hospitalar do HU. “Precisamos do diagnóstico mais precoce possível para orientar a conduta médica e evitar a disseminação do vírus dentro do hospital”, explica. “Se pudéssemos, faríamos o teste para todo mundo; mas no momento isso não é possível, então temos que definir para quais pacientes ele é mais urgente.”
Vários profissionais de saúde do HU que foram preventivamente afastados nas últimas semanas, por apresentarem algum sintoma respiratório, puderam voltar ao trabalho após o teste confirmar que eles não tinham a covid-19 — evitando, assim, que a equipe ficasse desfalcada de recursos humanos essenciais sem necessidade, segundo Valéria.
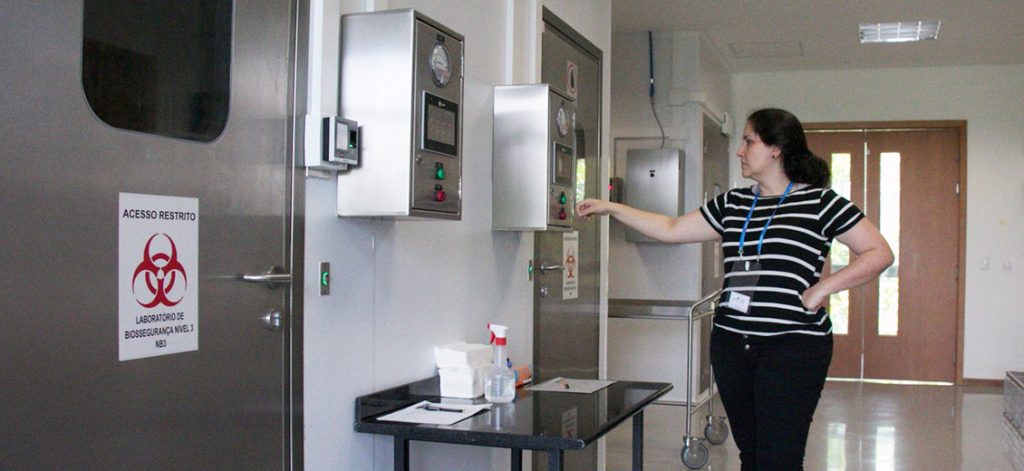
A virologista Ana Paula Vilela checa as condições de temperatura e pressão dentro do laboratório NB3 — Foto: Herton Escobar/USP Imagens
Técnica molecular
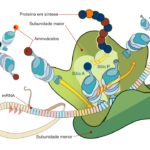
A técnica usada no diagnóstico molecular é a RT-PCR (Real-Time Polymerase Chain Reaction, ou reação em cadeia da polimerase em tempo real), que detecta a presença do material genético do vírus nas amostras. O primeiro passo é quebrar as células para liberar os vírus; depois, utiliza-se uma enzima (chamada transcriptase reversa) para converter o genoma do vírus de RNA para DNA. Em seguida, acrescenta-se à mistura uma sequência de DNA especialmente “programada” em laboratório (como se fosse um software) para detectar e replicar algum trecho específico do genoma do SARS-CoV-2, junto com moléculas fluorescentes que fazem essas cópias do DNA viral brilharem aos olhos de uma máquina.
O resultado aparece na tela do computador, na forma de um gráfico: se o vírus estiver presente na amostra, seu material genético será replicado milhões de vezes e a luz emitida pelas moléculas fluorescentes será registrada pelo sensor do aparelho como um sinal da infecção. Dependendo da intensidade dessa luz, é possível até estimar a quantidade de vírus presente no paciente. Se o vírus não estiver presente na amostra, não aparece nada.
Tudo isso acontece dentro de pequenos tubinhos e placas, envolvendo volumes ínfimos de substâncias, que precisam ser cuidadosamente medidos e misturados pelos pesquisadores. O procedimento pode ser feito dentro de um laboratório NB2, mas a recomendação da Sociedade Brasileira de Virologia (SBV) é que ele seja feito em NB3, com uma margem de segurança maior.
“Quanto mais testes a gente fizer, mais cedo a gente consegue identificar quem está infectado, isolar essas pessoas e quebrar a cadeia de transmissão”, descreve Paola. O gargalo, segundo ela, é a falta de reagentes — os ingredientes químicos e moleculares necessários para fazer a receita funcionar —, que são todos importados e estão em falta no mercado internacional, por conta da alta demanda imposta pela pandemia. Daí a opção de testar apenas profissionais de saúde, pacientes graves e pessoas que tiveram contato direto com eles.
“Temos um estoque para 3 mil testes, que estamos usando com cuidado para não faltar mais adiante, se a epidemia explodir”, diz Cunha, especialista em virologia molecular. A RUDIC está trabalhando com a Secretaria de Saúde do Estado de São Paulo para comprar novos reagentes o mais rápido possível, e então ampliar as equipes de análise nos laboratórios. A meta da rede é chegar a uma capacidade de realizar 45 mil testes moleculares por mês, o que permitiria absorver uma parte mais significativa da demanda de testagem do sistema público de saúde.
Esses testes permitem detectar o vírus já nos primeiros dias de infecção. O cenário ideal, segundo os especialistas, seria testar um grande número de pessoas, para identificar e isolar portadores assintomáticos o mais rápido possível, evitando que eles infectem outras pessoas sem saber que estão doentes.
Os chamados “testes rápidos”, que dão resultado em apenas alguns minutos — sem a necessidade de toda essa infraestrutura laboratorial e de biossegurança —, são importantes para monitorar o espalhamento do vírus na população, mas não substituem os testes moleculares na triagem hospitalar, segundo os especialistas.
Apesar de rápidos e práticos, esses testes são menos confiáveis (em termos de precisão do resultado) e identificam apenas a presença de anticorpos no sangue do paciente, em vez do próprio vírus. Ou seja, eles detectam uma resposta imunológica que já foi montada pelo organismo e que só é perceptível alguns dias após a infecção (num período que pode variar de 7 a 10 dias, dependendo do paciente e da sensibilidade do teste).
Consequentemente, a maioria daqueles que tiverem resultado positivo já estarão imunes ou na fase final da infecção, com poucas chances de transmitir o vírus para outras pessoas, segundo o pesquisador Luís Carlos Ferreira, diretor do Instituto de Ciências Biomédicas (ICB) da USP e co-coordenador da RUDIC e da PCPU.
Diante da emergência imposta pela pandemia, ele enviou no dia 20 de março uma mensagem aos docentes do ICB solicitando doações de reagentes, equipamentos e voluntários com experiência em RT-PCR para ajudar na realização dos testes moleculares de covid-19. “A resposta que recebemos foi impressionante”, conta Ferreira. “Recebemos centenas de mensagens, de toda a Universidade e até mesmo de fora da USP; todo mundo querendo ajudar.”
“Foi realmente fantástico, nunca vi esse nível de solidariedade em lugar nenhum”, reforça Paola. A PCPU recebeu mensagens de mais de 200 pessoas, alunos e professores, se oferecendo como voluntárias para o trabalho. Um processo de seleção e capacitação será feito nas próximas semanas para absorver essa ajuda, de acordo com o aumento da demanda (e a disponibilidade de reagentes).

Angélica Campos, Marielton Cunha e Ana Paula Vilela discutem os resultados dos testes que conduziram no dia anterior — Foto: Herton Escobar/USP Imagens
Pesquisas relacionadas
Além de ajudar na conduta dos hospitais, os exames geram informações importantes para a pesquisa científica da pandemia. Mesmo com todos os estudos que já vêm sendo feitos sobre o novo coronavírus nos últimos meses, em vários países, ainda há muita coisa que não se sabe sobre o comportamento dele dentro e fora do corpo humano.
Como ele evita ser detectado pelo sistema imunológico? Quais células e órgãos ele infecta, preferencialmente? Por que algumas pessoas são infectadas mais facilmente; e por que algumas desenvolvem sintomas mais ou menos graves do que as outras? Qual é a quantidade de vírus que as pessoas eliminam por diferentes vias, como secreções respiratórias e fezes? Depois que um paciente é curado e os sintomas da doença desaparecem, ele ainda pode transmitir o vírus? Por quanto tempo?
São algumas questões fundamentais que os cientistas ainda precisam solucionar, especialmente para a população brasileira, que é extremamente heterogênea e diferente geneticamente das populações asiáticas e europeias.
O cruzamento dos dados clínicos dos pacientes com os resultados dos testes moleculares e de outros exames realizados nos hospitais — como tomografias do pulmão e exames de sangue ou fezes — é uma ferramenta poderosa nesse tipo de investigação. Um dos casos investigados pelo grupo, por exemplo, é o de um núcleo familiar cuja mãe contraiu o SARS-CoV-2 mas aparentemente não passou para o marido nem o filho, mesmo convivendo com eles normalmente.
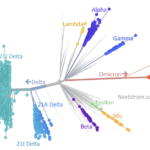
“Estamos trabalhando em duas frentes: diagnóstico e pesquisa”, explica o virologista Luiz Gustavo Góes, especialista em coronavírus e responsável pelo desenho experimental das pesquisas na plataforma. “A estrutura e a genética do SARS-CoV-2 são muito parecidas com as de outros coronavírus, mas a patogênese dele ainda não é muito conhecida.” Outra questão que a equipe planeja acompanhar no médio e longo prazo, segundo ele, é se o genoma do vírus está evoluindo (mudando) de alguma forma à medida que a epidemia avança no tempo e no espaço por diferentes regiões do País.
As linhas de investigação são muitas. “Nossa preocupação é justamente poder selecionar questões científicas que a gente possa resolver a partir do diagnóstico que estamos fazendo”, afirma Paola. “Fisicamente estamos muito cansados, mas intelectualmente, muito estimulados.”