Silvana Salles, Jornal da USP

Um funcionário público aposentado de 63 anos, morador de Belo Horizonte, chegou ao Hospital das Clínicas da Faculdade de Medicina de Ribeirão Preto da USP, no interior de São Paulo, com um quadro de saúde gravíssimo. Lutando contra o câncer desde 2017, ele já havia passado por radioterapia e quimioterapia, sem sucesso. A batalha parecia fadada à derrota quando os médicos conseguiram autorização para tentar uma nova terapia, que levou à remissão total da doença. Foi assim que o aposentado se tornou o primeiro paciente da América Latina tratado com células CAR T.
“Esse paciente é portador de um linfoma não Hodgkins avançado, uma doença agressiva. Ele já foi submetido a quatro linhas de tratamento prévias, teve uma resposta muito ruim, inclusive refratária a algumas delas, e veio justamente para fazer o CAR T-cell”, conta Renato Cunha, médico que cuida do caso em Ribeirão Preto. Cunha está à frente da tarefa de desenvolver uma plataforma brasileira de terapia com células CAR T no âmbito do Centro de Terapia Celular (CTC), um Centro de Pesquisa, Inovação e Difusão da Fundação de Amparo à Pesquisa do Estado de São Paulo (Fapesp) sediado na USP.
CAR T-cell, do inglês, significa “célula T com receptor de antígeno quimérico”. O complicado nome indica que o tratamento usa células geneticamente modificadas. Trata-se de uma terapia recente para combater o câncer. Nos Estados Unidos, a FDA (Food and Drug Administration, um órgão de vigilância sanitária semelhante à nossa Anvisa) liberou a terapia para uso comercial em 2018. Lá, como em outros países ricos, os resultados são tão promissores que renderam aos seus precursores o prêmio Nobel de Fisiologia e Medicina no ano passado.
“O câncer, todo mundo sabe, é um desafio. Os tratamentos têm melhorado muito e esse tratamento com as células CAR T é um dos mais promissores que existem no momento. É um tratamento disponível em poucos países”, afirma o médico hematologista Dimas Tadeu Covas, professor da Faculdade de Medicina de Ribeirão Preto (FMRP) da USP e coordenador do CTC. “Nós desenvolvemos uma tecnologia toda nossa, toda nacional, dentro de um instituto público, dentro de um hospital público, apoiado pela USP, pela Fapesp, pelo CNPq [Conselho Nacional de Desenvolvimento Científico e Tecnológico] e pelo Ministério da Saúde. Portanto, (é) um tratamento que se destina aos nossos pacientes do Sistema Único de Saúde (SUS)”, completa o professor.
O principal problema da terapia com células CAR T é o custo. Segundo Covas, nos EUA, a produção das células e as despesas hospitalares, juntas, chegam a custar US$ 1 milhão (mais de R$ 4 milhões). Covas calcula que a plataforma brasileira poderá baratear o tratamento em até 20 vezes, na comparação com o custo de um produto comercial. Além disso, a ideia é que o CTC mantenha aberto o protocolo de produção de células CAR T, permitindo que outros laboratórios reproduzam as técnicas para cuidar de mais pacientes.
“Representa um grande avanço científico, porque é um tratamento muito recente, uma tecnologia protegida por segredos industriais. E, por outro lado, é um grande avanço em termos sociais. Vamos poder oferecer isso, daqui a algum tempo, para a nossa população“, comemora o coordenador do CTC.
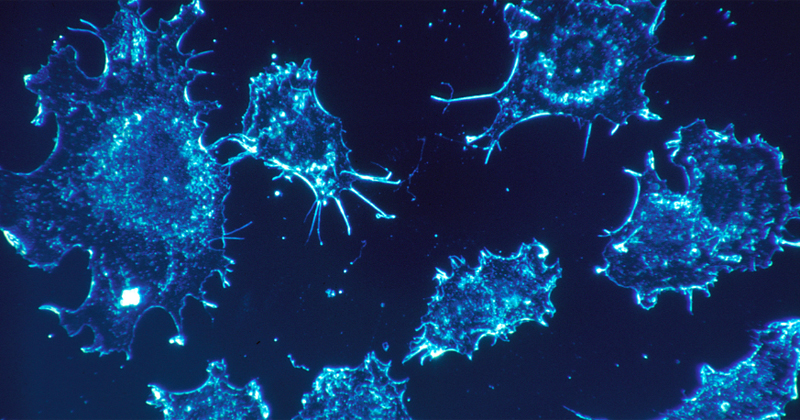
As células CAR T foram reintroduzidas no paciente e conseguiram reconhecer e destruir as células cancerosas – Foto: Células humanas – Wikimedia/National Cancer Institute
Como funcionam as células CAR-T?
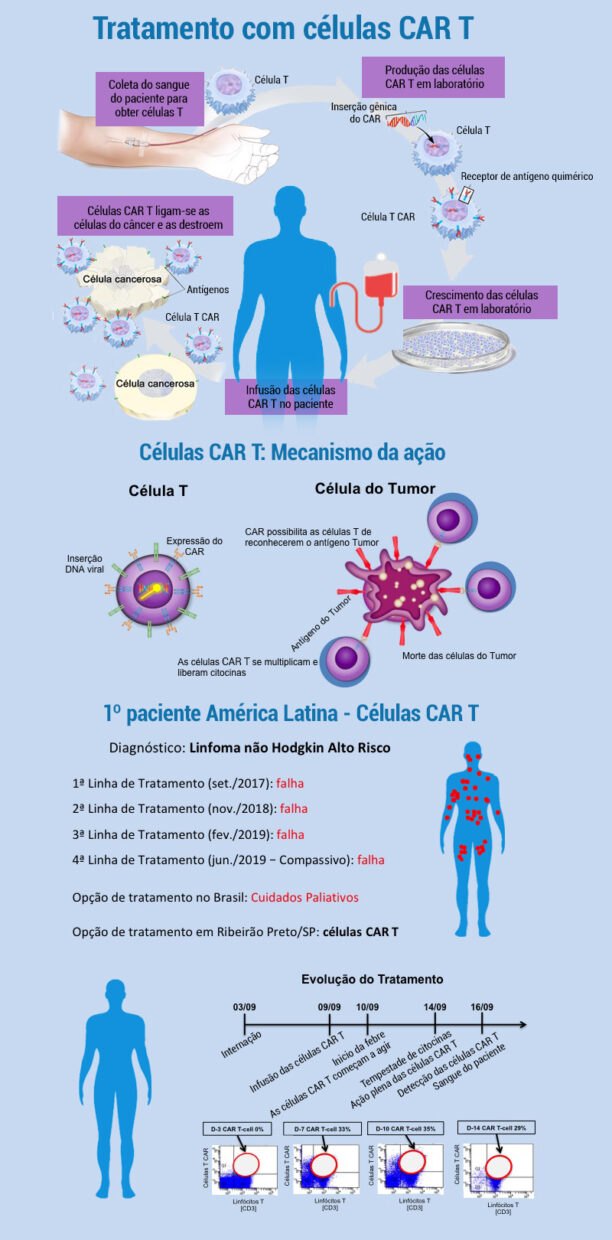
A terapia com células CAR T não é simples. Exige uma estrutura laboratorial complexa, certificada pela Anvisa e com boas práticas de produção. Exige também hospitais com capacidade para fazer transplantes de medula óssea, bons laboratórios e bom suporte de tratamento intensivo. Uma vez que as condições permitam, tudo começa com uma amostra de sangue do paciente.
Nosso sistema imunológico é composto majoritariamente de dois tipos de células especializadas. Um deles é o linfócito B, responsável por produzir anticorpos. O outro é o linfócito T, que funciona como um guarda do nosso organismo – é ele que ataca as bactérias invasoras, por exemplo. No caso do tratamento realizado em Ribeirão Preto, o câncer do paciente era causado por linfócitos B doentes. E o que os pesquisadores fizeram foi extrair os linfócitos T da amostra de sangue do paciente para modificá-los geneticamente.
No laboratório, eles introduziram nessas células um vetor – uma espécie de vírus sintético que carrega no DNA a habilidade de reconhecer determinadas substâncias de interesse. Os linfócitos T modificados ganharam, então, um receptor que lhes permite reconhecer o alvo terapêutico. Foi assim que os linfócitos T se tornaram células CAR T.
Posteriormente, as células CAR T foram reintroduzidas no paciente. Aqui, o alvo era uma proteína chamada CD-19. Como a proteína CD-19 está presente na membrana dos linfócitos B doentes, agora as células modificadas conseguiam reconhecer e destruir as células cancerosas.
Uso compassivo
Como os estudos clínicos do CTC com células CAR T ainda não estão abertos, o paciente mineiro conseguiu o tratamento na modalidade de uso compassivo. “No tratamento compassivo o paciente te procura e pede para ser tratado como última alternativa, porque ele não tem mais nenhuma opção. Geralmente, para fazer uso compassivo, é aquele paciente que poderia entrar em algum estudo clínico, mas ele não preenche critérios. Isso surgiu para ele não ficar sem tratamento”, explica Renato Cunha.
Foi justamente este o caso. A família do paciente havia entrado em contato com hospitais no exterior que fazem essa terapia, mas a burocracia envolvida e o alto custo do tratamento tornavam a viagem proibitiva. Eles descobriram o nome de Cunha por acaso, ao encontrar uma reportagem do final do ano passado que contava que o médico da USP havia ganho um prêmio da Sociedade Americana de Hematologia (ASH, em inglês) para desenvolver o processo de produção de células CAR T no Brasil.
“Ele escreveu para mim e eu respondi, falei para ele que a gente não estava com o protocolo (de estudo clínico) aberto. Mas ele falou, ‘olha eu gostaria muito de ir a Ribeirão conversar; mesmo que a gente não consiga fazer, eu gostaria de ter a sua opinião sobre o meu tratamento’”, relata o médico.
O aposentado e o filho foram a Ribeirão Preto conversar com Cunha e seguiram em contato com o médico depois. Eles tentaram o tratamento com uso compassivo de um medicamento chamado Polatuzumab, porém, quando o câncer se espalhou ainda mais, decidiram insistir na possibilidade do CAR compassivo. Por sorte, a equipe de Cunha havia recém-finalizado as etapas de validação laboratorial do processo de produção das células.
O paciente deu entrada no Hospital das Clínicas da FMRP no começo de setembro. Estava muito magro, tinha suor noturno, dor nos ossos e estava usando a dose máxima de morfina. Ele foi submetido a uma aplicação de células CAR T, teve uma reação inflamatória conhecida pelos médicos como “tempestade de citocinas” e ficou semanas em observação. A tempestade de citocinas foi um importante indicador de que as células CAR T haviam encontrado seu alvo. Mais de 30 dias depois, ele não apresenta mais sintomas clínicos nem laboratoriais da doença e deve receber alta no próximo sábado (12). “Ele tirou a morfina, não tem mais suor noturno, voltou a ganhar peso e a dor que ele sente é decorrente de uma fratura que ele teve nas costas por causa do linfoma”, conta o médico do CTC.
Cunha destaca que, dos testes feitos em laboratório com as células CAR T ao atendimento do paciente, tudo foi feito na cidade do interior de São Paulo, o que demonstra que os pesquisadores conseguiram dominar o processo. Agora, poderão se dedicar a testar outros vetores, outros alvos terapêuticos e criar um produto que possa ser adotado pelo SUS.
“É como, por exemplo, produzir uma aspirina. Você aprende a produzir um comprimido. Naquele momento aspirina, mas depois pode ser um anador, pode ser um tilenol. O importante é você ter essa tecnologia feita e bem adaptada ao nosso cenário. É importante dizer isso, porque a gente agora tem uma independência, a gente tem a tecnologia que a gente precisa”, diz o médico.