José Tadeu Arantes, Agência Fapesp
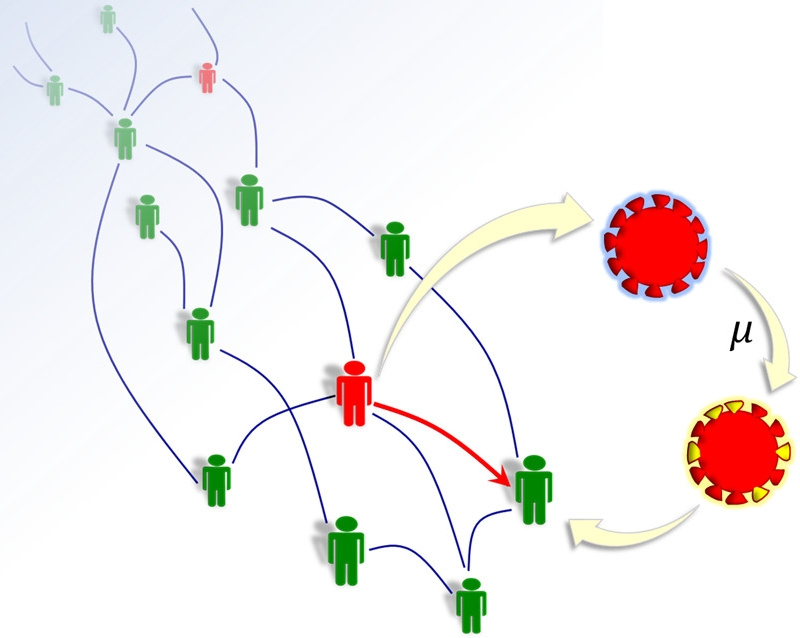
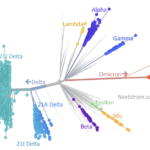
Trabalho foi divulgado na revista PLOS ONE. Equações sugerem ser possível estimar a variabilidade da população viral com base em dados epidemiológicos (imagem: acervo dos pesquisadores)
As mutações do SARS-CoV-2 são um dos temas mais quentes do momento. As novas variantes do vírus estão fazendo com que a pandemia de covid-19 recrudesça em lugares onde parecia controlada. E podem prolongar a fase crítica atual muito além do tempo esperado.
Um estudo, realizado no Instituto de Física Gleb Wataghin, da Universidade Estadual de Campinas (IFGW-Unicamp), modelou as mutações sofridas pelo SARS-CoV-2 durante seu processo de replicação e, por decorrência, a evolução genética do vírus ao longo da pandemia. Os dados foram publicados na revista PLOS ONE.
No artigo, os autores enfatizam o alerta já feito por outros cientistas: as populações que não estão sendo vacinadas e os grupos sociais que se recusam a receber a vacina favorecem o aparecimento de variantes. E, se esse problema não for resolvido urgentemente, a pandemia pode ter um novo pico em escala global.
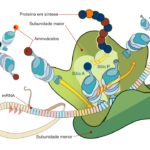
“Como se sabe, os vírus são organismos muito simples, incapazes de se reproduzir por si mesmos. Para poderem replicar o seu RNA, precisam utilizar as células do hospedeiro. E, ao danificá-las, causam a doença. Ocorre que, durante o processo de replicação, erros de cópia são inevitáveis. Os organismos mais complexos possuem mecanismos para correção de erros. Mas os vírus não possuem. Caso algum desses erros proporcione uma vantagem ao vírus em termos de propagação, essa mutação passará a ter importância. E, eventualmente, poderá até predominar. Se a propagação ocorre sem freios, devido à não vacinação, as mutações tendem a acontecer cada vez mais e a se espalhar pelo globo”, diz o físico Marcus de Aguiar, professor do IFGW-Unicamp e coordenador do estudo.
Ao contrário do que dizem os negacionistas, não é a vacinação que favorece a mutação. Mas a falta dela, explica o pesquisador.
“Quando se vacina grande parte da população, o vírus para de circular. E, circulando menos, diminui a taxa de reprodução viral. E, portanto, a chance de aparecerem novas variantes.”
Os modelos tradicionais de epidemiologia enfocam os números de pessoas infectadas, suscetíveis e recuperadas ao longo do tempo. No estudo em pauta, o modelo incluiu a descrição do RNA do vírus. “Saber quão diferentes são os microrganismos em circulação em relação aos vírus originais é importante para entender o aparecimento de novas variantes. Também para estimar se, mesmo que já tenha sido infectada pelo vírus original, uma pessoa poderá vir a ser reinfectada pela variante. E, ainda, para prever se o novo patógeno poderá escapar ou não da ação de vacinas projetadas para o original”, explica Aguiar.
Como acontece com todo modelo científico, o modelo desenvolvido no estudo é uma aproximação idealmente simplificada daquilo que de fato acontece na realidade. A base a partir da qual ele foi construído é o modelo do tipo SEIR, já consagrado em epidemiologia. A sigla SEIR é formada pelas letras iniciais de quatro palavras em língua inglesa: “Susceptible” (Suscetível), “Exposed” (Exposto), “Infectious” (Infectante) e “Recovered” (Recuperado). “Suscetível” é a pessoa que pode ser infectada; “exposta”, a infectada, mas não infectante; “infectante”, a infectada e infectante; “recuperada”, aquela que já se recuperou da doença e, idealmente, não poderia ser mais infectada.
“Para evitar uma complexidade excessiva, que tornaria o modelo matematicamente inviável, consideramos que indivíduos classificados como ‘recuperados’ não podem ser infectados por nenhuma variante que possa surgir. Também consideramos as mutações como neutras, ou seja, que não conferem ao vírus mutado nenhuma vantagem ou desvantagem adicional em relação ao vírus que lhe deu origem. Não é isso que acontece de fato na realidade. Mas adotamos essas simplificações para poder concentrar o foco em nosso objetivo, que era estudar o acúmulo das mutações virais durante a pandemia e o quão diferentes os vírus podem ficar”, esclarece o pesquisador.
Para atingir esse objetivo, o modelo foi acrescido de uma descrição dos vírus, a partir de seu RNA, com 29.900 bases nitrogenadas, e uma taxa de mutação 0,001 por base por ano – dados esses obtidos a partir da estrutura e do comportamento do SARS-CoV-2.
“Enquanto um indivíduo permanece infectado, o vírus pode sofrer mutações e ser transmitido. Calculamos a ‘distância’ entre o vírus original e a variante a partir do número de bases nitrogenadas distintas que eles apresentam. Nossas equações sugerem que é possível prever, com dados epidemiológicos [número de suscetíveis, infectados e recuperados], a variabilidade da população viral [‘distância média’ entre as sequências de RNA], sem que seja necessário ter acesso a uma enorme quantidade de dados genéticos”, diz Aguiar.
Com o intuito de testar o modelo, os pesquisadores utilizaram as equações para mostrar, a partir dos dados da epidemia na China, no início de 2020, como seria a evolução da “distância genética média” entre os vírus que teriam hipoteticamente surgido durante aquele período. Comparando o resultado com as distâncias calculadas a partir de dados genéticos obtidos localmente no mesmo período, a previsão apresentou boa concordância com os dados reais.
“A propagação do vírus através de comunidades distintas [cidades, países etc.] pode levar a sequências bastante diferentes da original, aumentando as chances de reinfecção, dependendo fortemente da conectividade entre essas comunidades. Quanto menos conectadas duas comunidades, maior a diferença no vírus que uma pode transmitir para a outra. Isso aumenta a chance de que o vírus circulante em uma das comunidades seja capaz de escapar do controle do sistema imune dos indivíduos da outra comunidade”, resume o pesquisador.
E acrescenta: “É importante ressaltar que, para que ocorra a mutação efetiva do vírus, conferindo-lhe vantagens ou desvantagens, é necessário que os defeitos de replicação ocorram em locais específicos do RNA viral. Assim, distâncias genéticas altas aumentam a chance de que existam mutações importantes, mas não as garantem. E nossas considerações são baseadas nessa perspectiva”.
O estudo recebeu apoio da Fundação de Amparo à Pesquisa do Estado de São Paulo (Fapesp) por meio de um Projeto Temático; de um Auxílio à Pesquisa Regular concedido a Aguiar; e da Bolsa de Doutorado de Vitor Marquioni Monteiro, orientando de Aguiar e autor principal do artigo.
O artigo Modeling neutral viral mutations in the spread of SARS-CoV-2 epidemics pode ser acessado em https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0255438.