(Este texto dá continuidade à série A Beleza Invisível da Biodiversidade, tratando do gênero Erythrina, nome genérico de um conjunto de plantas pertencentes a família Fabaceae).
Erythrina deriva da palavra grega erythros, que significa vermelho, cor que aparece brilhante nas lindas flores das plantas que o nome abarca. Árvore de coral, árvore de chama, são denominações populares para o gênero típico das regiões tropicais e subtropicais, portanto, de ocorrência em todo o mundo.
Plantas desta espécie são árvores que podem alcançar até 30 metros de altura. A denominação árvore de coral certamente deve-se ao fato de os ramos das flores num vermelho brilhante assemelharem-se às forma do Corallium rubrum, um coral marinho muito bonito. Em geral, plantas de uso tradicional recebem muitos nomes populares, dados geralmente em função dos locais de ocorrência e características de cada espécie. No Brasil, são encontradas sete espécies de Erythrina: E. verna, E. velutina, E. crita-galli, E. poeppigiana, E. fusca, E. falcata, E. speciosa.
A espécie Erythrina verna, também conhecida por mulungu (Figura 1) chega a alcançar 14 metros de altura. De ocorrência frequente nas florestas da bacia do Rio Paraná e nas regiões de Cerrado da região oeste do Estado de São Paulo e Triângulo Mineiro, sua entrecasca é utilizada pela população dessas regiões como calmante e sedativo. Há registro também do uso popular como laxante.

Figura 1. Flores de Erythrina verna (mulungu), Fabaceae, planta utilizada na medicina popular como calmante e sedativo
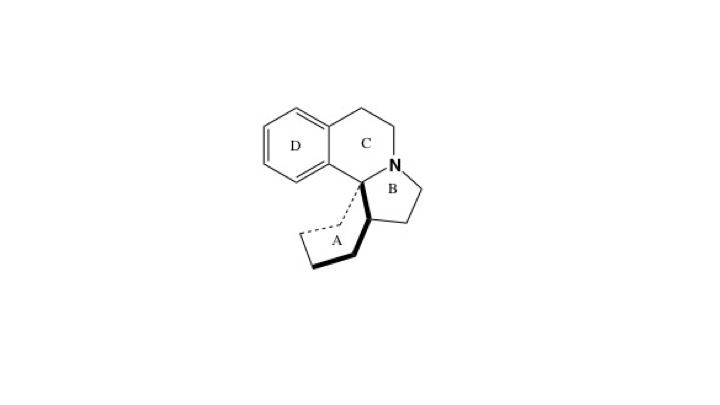
Os alcaloides (substâncias orgânicas nitrogenadas de plantas) da classe dos isoquinolínicos são os marcadores químicos do gênero Erythrina, de onde foram isolados mais de 100 derivados, cuja estrutura básica (Figura 2) caracteriza todos como alcaloides eritrínicos.
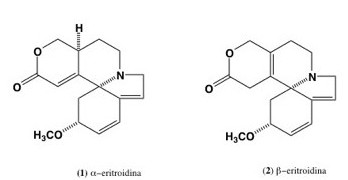
Em 1877 os estudos farmacológicos conduzidos pelos pesquisadores Domínguez e Altamirano com um extrato produzido a partir das sementes da E. americana revelaram uma ação paralisante muscular, semelhante aos efeitos da d-tubocurarina um produto natural, extraído de Chondodendron tomentosum, família Menispermaceae. A partir de então, várias pesquisas fitoquímicas e farmacológicas vêm sendo feitas com extratos preparados de diferentes espécies de Erythrina. A eritroidina (1) isolada por Folkers e Major (1937) foi identificada como o principio responsável pela atividade curarizante, observado no extrato das sementes de E. Americana, posteriormente identificadas como uma mistura de isômeros a-eritroidina (1) e b-eritroidina (2). Sendo o isômero 2 responsável pela atividade colinérgica, devido à sua capacidade de antagonizar receptores nicotínicos periféricos. Importante ressaltar que E. verna (mulungu) é uma espécie de uso tradicional em várias partes do mundo e no Brasil, dado as propriedades ansiolíticas.
No Brasil já é comercializada como fitoterápico. Em março de 2009, o Ministério da Saúde (MS), por meio do Programa Nacional de Plantas Medicinais e Fitoterápicos, lançou uma lista de 71 plantas medicinais de interesse do SUS e a E. verna (mulungu) está listada devido ao conhecimento tradicional de uso como ansiolíticas.
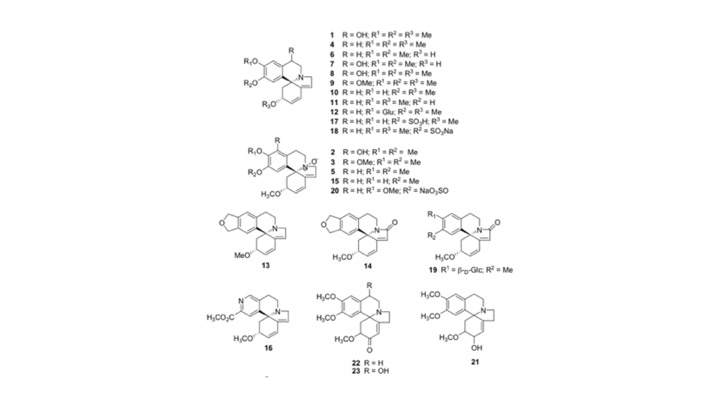
Após o isolamento de α e β-eritroidina de E. americana e das descobertas de suas propriedades farmacológicas, houve grande interesse no estudo fitoquímico de muitas outras espécies de Erythrina, o que levou a identificação de inúmeros alcaloides eritrínicos (Figura 3).
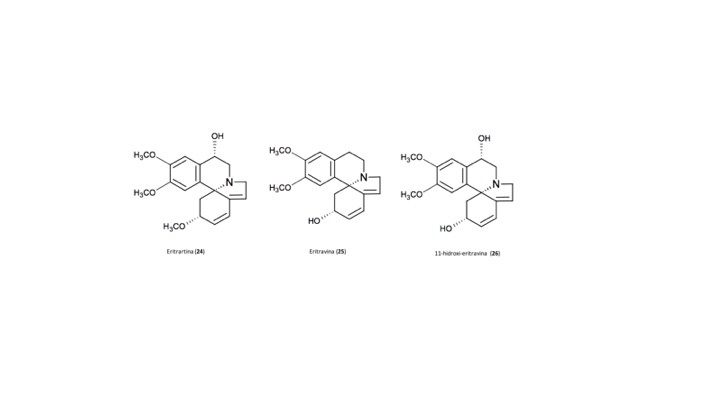
Pesquisas realizadas no NuBBE com E. Mulungu levou ao isolamento, identificação dos alcaloides eritrartina (24), (+)-eritravina (25) e (+)-11-α-hidroxierisotrina (26) presentes no extrato hidro alcoólico ativo das flores de E. Verna, e à confirmação das propriedades ansiolíticas destes alcaloides, corroborando o uso popular da espécie.
A beleza visual das eritrinas sem folhas e cobertas de flores brilhantes e vermelhas podem ser vistas nesta época do ano em praças, jardins, na mata e no cerrado e os arranjos moleculares dos inúmeros alcaloides confirmam que a “planta de coral” é de fato bela por fora e por dentro.
—————————————————————————————–
Vanderlan da S. Bolzani é professora titular do IQAr-UNESP, membro da Coordenação Biota e vice-diretora da SBPC
Referências
AGUILAR, M. I.; GIRAL, F.; ESPEJO, O. Alkaloids from the flowers of Erythrina americana. Phytochemistry. v.20. n.8, p.2961-2962. 1981.
AHMAD, V. U.; NAJMUS-SAQIB, Q.; USMANGHANI, K.; MIANA, G. A. Isolation of erysotrine and 11-hydroxy-erysothrine from the leaves of Erythrina herbacea Linn. Journal of the Chemical Society of Pakistan, v. 1, n. 1, p. 79-80. 1979.
BOEKELHEIDE, V.; GRUNDON, M. F. A characterization of α-erythroidine. Journal of the American Chemical Society, v. 75, n. 11, p. 2563- 2566. 1953.
BOEKELHEIDE, V.; WEINSTOCK, J.; GRUNDON, M. F.; SAUVAGE, G. L.; AGNELLO, E. J. The structure of β-erythroidine and its derivatives. Journal of the American Chemical Society, v. 75, n. 11, p. 2550-2558, 1953.
BORCHARDT, J. K. The beginnings of drug therapy: Ancient Mesopotamian Medicine. Drug News & Perspectives, v.15. n. 3. p.187-192, 2002.
FLAUSINO, O. A. JR.; PEREIRA, A. M.; BOLZANI, V. S.; NUNES-DE-SOUZA, R. L. Effects of Erythrinian alkaloids isolated from Erythrina mulungu (Papilionaceae) in mice submitted to animal models of anxiety. Biological and Pharmaceutical Bulletin, v.30, p.375-378, 2007a.
FLAUSINO, O. A. JR.; SANTOS, L. A.; VERLI, H.; PEREIRA, A. M.; BOLZANI, V. S.; NUNES-DE-SOUZA, R. L. Anxiolytic effect of erythinian alkaloids from Erythrina mulungu. Journal of Natural Products. v. 70, p. 48-53, 2007b.
FOLKERS, K.; KONIUSZY, F. Erythrina alkaloids VII – Isolation and characterization of the new alkaloids, erythraline and erythrartine. Journal of the American Chemical Society, v.62, p.437, 1940
FOLKERS, K.; MAJOR, R. T. Isolation of erythroidine, an alkaloid of curare action, from Erythrina americana Mill. Journal of the American Chemical Society, v.59, p.1580, 1937.